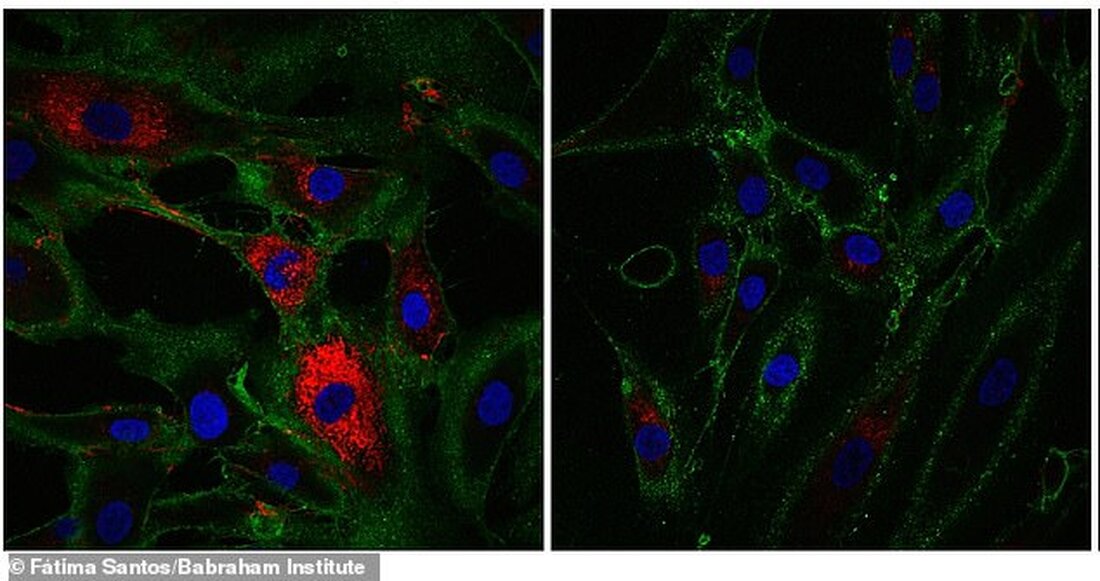
لقد كان حلم النساء – والرجال – لعدة قرون. يقول العلماء الآن أنهم وجدوا طريقة لعكس عملية الشيخوخة في جلد الإنسان.
كشف باحثون في كامبريدج أنهم أعادوا برمجة خلايا الجلد من أشخاص تتراوح أعمارهم بين 38 و53 عامًا لجعلهم "أصغر سنًا" بـ 30 عامًا.
يعمل هذا الإجراء على إرجاع ساعة الشيخوخة إلى الوراء أكثر من إجراءات إعادة البرمجة السابقة دون الإضرار بالخلايا.
ويقول الباحثون إن بإمكانهم استعادة الوظائف التي فقدتها في الخلايا القديمة جزئيًا.
وفي حين أن البحث لا يزال في مراحله الأولى، فإن النتائج يمكن أن تُحدث ثورة في الطب التجديدي في نهاية المطاف، خاصة إذا كان من الممكن تكرارها في أنواع الخلايا الأخرى والأنسجة الأخرى في الجسم، كما يزعم الباحثون.
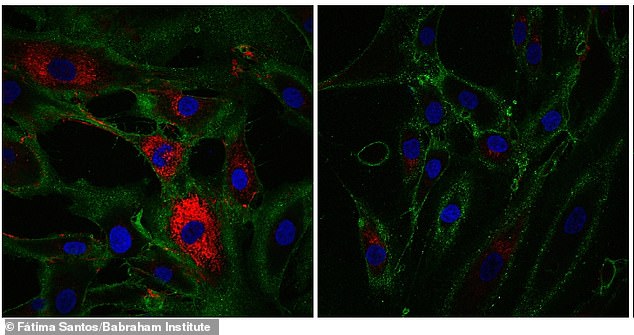
وفي التجارب، استعادت الخلايا المتقدمة في السن علامات مميزة لخلايا الجلد التي تنتج الكولاجين، وهو جزيء موجود في العظام وأوتار الجلد والأربطة يساعد في بناء الأنسجة وشفاء الجروح. هنا يظهر اللون الأحمر إنتاج الكولاجين بواسطة خلايا الجلد التي تسمى الخلايا الليفية
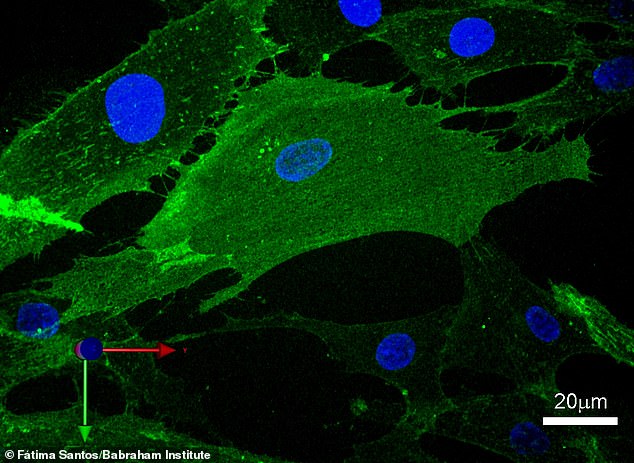
يتغير شكل الخلايا مؤقتًا أثناء إعادة البرمجة المؤقتة. تُظهر هذه الصورة خلية واحدة ذات علامات سطحية من الخلايا الليفية باللون الأخضر
شيخوخة الخلايا في التجاربأصبحت أشبه بخلايا الجلد التي تسمى الخلايا الليفية، والتي تنتج الكولاجين، وهو البروتين الذي يجمع الجسم معًا ويبقيه قويًا.
يتناقص عدد الخلايا الليفية في جلد الإنسان تدريجيًا مع تقدم العمر. وتتقلص هذه الخلايا أيضًا مع تقدمنا في العمر.
ويقول الباحثون إن النتائج الجديدة يمكن أن تؤدي إلى نهج مستهدف لعلاج الشيخوخة يمكن أن يحدث "ثورة" في الطب التجديدي.
تم إجراء البحث الجديد في معهد بابراهام، وهو معهد أبحاث علوم الحياة في كامبريدج، ونشر في المجلة eLife.
وقال الدكتور ديلجيت جيل من معهد بابراهام: "تمثل نتائجنا تقدما كبيرا في فهمنا لإعادة برمجة الخلايا".
"لقد أثبتنا أنه يمكن تجديد الخلايا دون أن تفقد وظيفتها، وأن التجديد يهدف إلى استعادة بعض الوظائف للخلايا القديمة.
"إن حقيقة أننا شهدنا أيضًا انعكاسًا لمؤشرات الشيخوخة في الجينات المرتبطة بالأمراض يعد أمرًا واعدًا بشكل خاص لمستقبل هذا العمل."
مع تقدم العمر، تتناقص وظائف الخلايا ويصبح الجينوم - مخطط الحمض النووي الخاص بها - غنيًا بعلامات الشيخوخة.
تهدف البيولوجيا التجديدية إلى إصلاح الخلايا أو استبدالها، حتى القديمة منها.
إحدى أهم الأدوات في علم الأحياء التجديدي هي قدرتنا على إنشاء خلايا جذعية "مستحثة".
ومع ذلك، فإن هذه العملية تؤدي بشكل أساسي إلى محو الخلايا من وظيفتها، مما يمنحها القدرة على أن تصبح أي نوع من الخلايا.
ينبع هذا العمل في الأصل من العمل الذي أجراه معهد روزلين في إدنبره في التسعينيات لتحويل خلية ثديية مأخوذة من خروف يبلغ من العمر ست سنوات إلى جنين.
أدى هذا المشروع إلى إنشاء النعجة دوللي، وهي أول حيوان ثديي يتم استنساخه من خلية جسدية بالغة.
وأظهر ابتكار دوللي أن الجينات الموجودة في نواة الخلية الناضجة لا تزال قادرة على العودة إلى حالة الجنين الكاملة، مما يعني أن الخلية يمكن أن تنقسم لإنتاج جميع خلايا الحيوان المختلفة.

ولدت النعجة دوللي (في الصورة) في يوليو 1996 في معهد روزلين في إدنبرة. وقد تمت زراعته من خلية ثديية لخروف عمره ست سنوات
وهذا ما مهد الطريق أمام العالم الدكتور شينيا ياماناكا الحائز على جائزة نوبل، والذي أصبح في عام 2007 أول عالم يحول الخلايا الطبيعية التي لها وظيفة محددة إلى خلايا جذعية لها قدرة خاصة على التطور إلى أي نوع من الخلايا.
تستغرق هذه الطريقة، التي تسمى IPS، حوالي 50 يومًا وتستخدم أربعة جزيئات رئيسية تسمى عوامل النسخ ياماناكا - Oct4، وSox2، وKlf4، وcMyc.
الطريقة الجديدة لمعهد بابراهام، والتي تسمى إعادة البرمجة العابرة لمرحلة النضج، تعرض الخلايا لعوامل ياماناكا لمدة 13 يومًا فقط بدلاً من 50 يومًا.
وفي هذه المرحلة، لم تكن الخلايا قد تحولت بعد إلى خلايا جذعية جنينية، بل تم "تجديد شبابها" كما لو كانت أصغر بـ 30 عامًا.
مُنحت الخلايا المعاد برمجتها جزئيًا وقتًا لتنمو في ظل ظروف طبيعية لمراقبة ما إذا كانت وظيفة خلايا الجلد المحددة قد عادت أم لا.
أظهر التحليل الجينومي أن الخلايا استعادت علامات مميزة لخلايا الجلد (الخلايا الليفية)، وهو ما تم تأكيده من خلال مراقبة إنتاج الكولاجين في الخلايا المعاد برمجتها.
ولإظهار أن الخلايا قد تجددت، بحث الباحثون عن التغيرات في خصائص الشيخوخة.

يتضمن البحث ما يسمى بعوامل النسخ ياماناكا، والتي سميت على اسم العالم الياباني الحائز على جائزة نوبل الدكتور شينيا ياماناكا (في الصورة).
قام الباحثون بفحص عدة مقاييس لعمر الخلية. الأول هو الساعة اللاجينية، حيث تشير العلامات الكيميائية الموجودة في جميع أنحاء الجينوم إلى العمر.
والثاني هو النسخ، أي جميع قراءات الجينات التي تنتجها الخلية.
وقال الفريق إنه من خلال هذين المقياسين، تطابقت الخلايا المعاد برمجتها مع خصائص الخلايا التي كانت أصغر بـ 30 عامًا مقارنة بمجموعات البيانات المرجعية.
لا يمكن ترجمة هذه التقنية على الفور إلى بيئة سريرية لأن مرض باركنسون يزيد من خطر الإصابة بالسرطان.
في الوقت الحالي، تتمثل خطوات البحث التالية في فهم الآلية الدقيقة التي جعلت إعادة البرمجة الجزئية هذه ممكنة، ولكن في النهاية يمكن استخدامها لعلاجات الخلايا في الحالات التي يُحدث فيها عمر الخلايا فرقًا، مثل: ب. في شفاء الجلد من الحروق.
تعتمد التطبيقات المحتملة لهذه التقنية على ظهور الخلايا ليس فقط أصغر سنًا، بل أيضًا على عملها مثل الخلايا الشابة.
تنتج الخلايا الليفية الكولاجين، وهو جزيء موجود في العظام وأوتار الجلد والأربطة التي تساعد على بناء الأنسجة وشفاء الجروح.
ووجد الباحثون في معهد بابراهام أن الخلايا الليفية المتجددة أنتجت المزيد من بروتينات الكولاجين مقارنة بالخلايا الضابطة التي لم تخضع لعملية إعادة البرمجة.
تنتقل الخلايا الليفية أيضًا إلى المناطق التي تحتاج إلى إصلاح، لذلك اختبر الباحثون الخلايا التي تم تجديدها جزئيًا عن طريق إنشاء قطع اصطناعي في طبقة من الخلايا في طبق.
ووجدوا أن الخلايا الليفية المعالجة انتقلت إلى الفجوة بشكل أسرع من الخلايا القديمة، وهي علامة واعدة على أنه يمكن في يوم من الأيام إنشاء خلايا أفضل في شفاء الجروح.
ويريد الباحثون أيضًا معرفة ما إذا كانت الطريقة الجديدة تعمل على أنسجة أخرى مثل العضلات والكبد وخلايا الدم.
وفي المستقبل، يمكن لهذا البحث أيضًا أن يفتح إمكانيات علاجية أخرى؛ ولاحظ الباحثون أن طريقتهم كان لها أيضًا تأثيرات على الجينات الأخرى المرتبطة بالأمراض والأعراض المرتبطة بالعمر.
أظهر جين APBA2، المرتبط بمرض الزهايمر، وجين MAF، الذي يلعب دورًا في تطور إعتام عدسة العين، تغيرات نحو مستويات النسخ الشبابية.

يمكن أن تؤدي النتائج الجديدة إلى نهج مستهدف لعلاج الشيخوخة والذي يمكن أن "يحدث ثورة" في الطب التجديدي (صورة أرشيفية)
إن الآلية الكامنة وراء إعادة البرمجة المؤقتة الناجحة لم يتم فهمها بالكامل بعد، وهي الجزء التالي من اللغز الذي يجب استكشافه.
ويتكهن الباحثون بأن المناطق الرئيسية من الجينوم المشاركة في تكوين هوية الخلية قد تفلت من عملية إعادة البرمجة.
قال البروفيسور وولف ريك، قائد مجموعة في برنامج أبحاث علم الوراثة اللاجينية والذي انتقل مؤخرًا لقيادة معهد ألتوس لابز كامبريدج: "هذا العمل له آثار مثيرة للغاية.
"قد نكون قادرين على تحديد الجينات التي تتجدد دون إعادة برمجتها واستهدافها للحد من آثار الشيخوخة.
"يعد هذا النهج باكتشافات قيمة يمكن أن تفتح آفاقًا علاجية مذهلة."
يقول البروفيسور ريك بي بي سي أن مصطلحات إكسير الشباب أو حبوب مكافحة الشيخوخة ليست سخيفة تمامًا.
وقال: "لقد تم استخدام هذه التقنية على الفئران المعدلة وراثيا، وهناك بعض علامات التجدد".
"أظهرت إحدى الدراسات علامات تجديد البنكرياس، وهو أمر مثير للاهتمام لقدرته على مكافحة مرض السكري."

 Suche
Suche
 Mein Konto
Mein Konto