Det har været kvinders – og mænds – drøm i århundreder. Nu siger videnskabsmænd, at de har fundet en måde at vende ældningsprocessen i menneskelig hud.
Forskere i Cambridge afslører, at de har omprogrammeret hudceller fra mennesker i alderen 38 og 53 for at gøre dem 30 år "yngre".
Proceduren skruer det aldrende ur længere tilbage end tidligere omprogrammeringsprocedurer uden at beskadige cellerne.
Forskere siger, at de endda delvist kan genoprette funktioner, der gik tabt i ældre celler.
Mens forskningen stadig er i sine tidlige stadier, kan resultaterne i sidste ende revolutionere regenerativ medicin, især hvis de kan replikeres i andre celletyper og andre væv i kroppen, hævder forskerne.
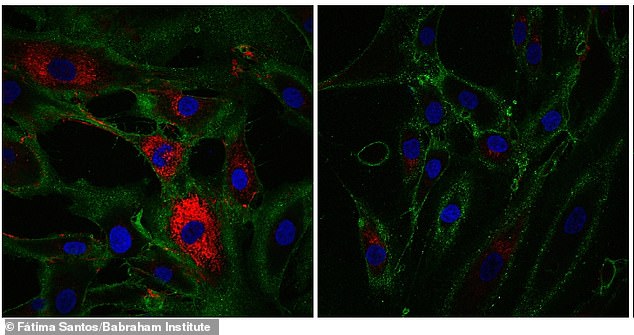
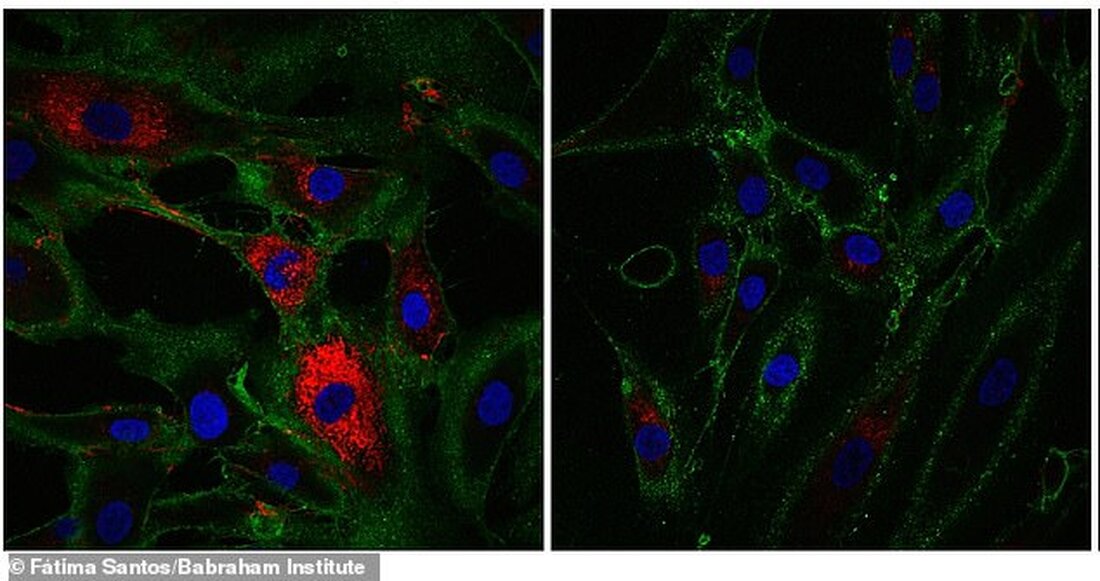
I eksperimenter havde aldrende celler genvundet markører, der er karakteristiske for hudceller, der producerer kollagen, et molekyle, der findes i knogler, hudsener og ledbånd, der hjælper med at strukturere væv og hele sår. Her viser rød kollagenproduktion af hudceller kaldet fibroblaster
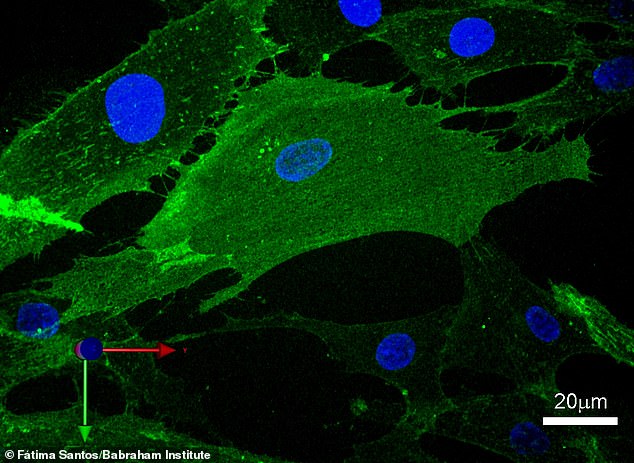
Celler ændrer midlertidigt form under midlertidig omprogrammering. Dette billede viser en enkelt celle med fibroblastoverflademarkører i grønt
Ældrende celler i eksperimenterblev mere som hudceller kaldet fibroblaster, som producerer kollagen, et protein, der holder kroppen sammen og holder den stærk.
Antallet af fibroblaster i menneskelig hud falder gradvist med alderen. Disse celler krymper også, når vi bliver ældre.
De nye resultater kan føre til en målrettet tilgang til behandling af aldring, der kan "revolutionere" regenerativ medicin, siger forskere.
Den nye forskning blev udført på Babraham Institute, et biovidenskabsforskningsinstitut i Cambridge, og offentliggjort i tidsskriftet eLife.
"Vores resultater repræsenterer et stort fremskridt i vores forståelse af celleomprogrammering," sagde Dr. Diljeet Gill fra Babraham Institute.
"Vi har bevist, at celler kan forynges uden at miste deres funktion, og at foryngelse sigter mod at genoprette nogle funktioner til gamle celler.
"Det faktum, at vi også så en vending af aldringsindikatorer i sygdomsassocierede gener, er særligt lovende for fremtiden for dette arbejde."
Med stigende alder falder cellernes funktionalitet, og genomet - deres DNA-plan - bliver beriget med tegn på ældning.
Regenerativ biologi har til formål at reparere eller erstatte celler, selv gamle.
Et af de vigtigste værktøjer inden for regenerativ biologi er vores evne til at skabe "inducerede" stamceller.
Men denne proces sletter i det væsentlige cellerne af deres funktion, hvilket giver dem potentialet til at blive en hvilken som helst celletype.
Arbejdet stammer oprindeligt fra arbejdet på Roslin Institute i Edinburgh i 1990'erne med at omdanne en brystcelle taget fra et seks år gammelt får til et embryo.
Dette projekt førte berømt til skabelsen af fåret Dolly, det første pattedyr klonet fra en voksen somatisk celle.
Dollys skabelse viste, at gener i kernen af en moden celle stadig er i stand til at vende tilbage til en embryonal totipotent tilstand - hvilket betyder, at cellen kan dele sig for at producere alle et dyrs forskellige celler.

Fåret Dolly (billedet) blev født i juli 1996 på Roslin Institute i Edinburgh. Det blev dyrket fra en brystcelle fra et seks år gammelt får
Dette banede vejen for den nobelprisvindende videnskabsmand Dr. Shinya Yamanaka, som i 2007 blev den første videnskabsmand til at omdanne normale celler, der har en bestemt funktion, til stamceller, der har den særlige evne til at udvikle sig til enhver celletype.
Denne metode, kaldet IPS, tager omkring 50 dage og bruger fire nøglemolekyler kaldet Yamanaka-transskriptionsfaktorer - Oct4, Sox2, Klf4 og cMyc.
Babraham Institutes nye metode, kaldet Maturation Phase Transient Reprogramming, udsætter celler for Yamanaka-faktorer i kun 13 dage i stedet for 50 dage.
På dette tidspunkt var cellerne endnu ikke blevet til embryonale stamceller, men blev "forynget", som om de var 30 år yngre.
De delvist omprogrammerede celler fik tid til at vokse under normale forhold for at observere, om deres specifikke hudcellefunktion vendte tilbage.
Den genomiske analyse viste, at cellerne havde genvundet markører, der er karakteristiske for hudceller (fibroblaster), hvilket blev bekræftet ved at observere kollagenproduktion i de omprogrammerede celler.
For at vise, at cellerne var blevet forynget, ledte forskerne efter ændringer i aldersegenskaberne.

Forskningen omfatter såkaldte Yamanaka-transskriptionsfaktorer, opkaldt efter den nobelprisvindende japanske videnskabsmand Dr. Shinya Yamanaka (billedet).
Forskerne undersøgte flere mål for cellealderen. Den første er det epigenetiske ur, hvor kemiske mærker til stede i hele genomet indikerer alder.
Det andet er transkriptomet, alle genudlæsninger produceret af cellen.
Gennem disse to foranstaltninger matchede de omprogrammerede celler profilen af celler, der var 30 år yngre sammenlignet med referencedatasæt, sagde holdet.
Teknikken kan ikke umiddelbart oversættes til en klinisk ramme, fordi PD øger risikoen for kræft.
For nu er de næste forskningstrin at forstå den nøjagtige mekanisme, der gjorde denne delvise omprogrammering mulig, men i sidste ende kunne den bruges til celleterapier i situationer, hvor cellernes alder gør en forskel, såsom: B. i hudheling fra forbrændinger.
Potentielle anvendelser af denne teknik afhænger af, at cellerne ikke kun ser yngre ud, men også fungerer som unge celler.
Fibroblaster producerer kollagen, et molekyle, der findes i knogler, hudsener og ledbånd, der hjælper med at strukturere væv og hele sår.
De foryngede fibroblaster producerede flere kollagenproteiner sammenlignet med kontrolceller, der ikke havde gennemgået omprogrammeringsprocessen, fandt Babraham Institute-forskere.
Fibroblaster bevæger sig også ind i områder, der skal repareres, så forskerne testede de delvist foryngede celler ved at skabe et kunstigt snit i et lag af celler i en skål.
De fandt ud af, at deres behandlede fibroblaster bevægede sig hurtigere ind i hullet end ældre celler – et lovende tegn på, at der en dag kunne skabes celler, der er bedre til at hele sår.
Forskerne vil også se, om den nye metode virker på andre væv som muskel-, lever- og blodceller.
I fremtiden kan denne forskning også åbne op for andre terapeutiske muligheder; Forskerne observerede, at deres metode også havde virkninger på andre gener forbundet med aldersrelaterede sygdomme og symptomer.
APBA2-genet, som er forbundet med Alzheimers sygdom, og MAF-genet, som spiller en rolle i udviklingen af grå stær, viste begge ændringer i retning af ungdommelige transkriptionsniveauer.

De nye resultater kan føre til en målrettet tilgang til behandling af aldring, der kan "revolutionere" regenerativ medicin (filfoto)
Mekanismen bag vellykket midlertidig omprogrammering er endnu ikke fuldt ud forstået og er den næste brik i puslespillet, der skal udforskes.
Forskerne spekulerer i, at nøgleområder i genomet, der er involveret i dannelsen af celleidentitet, kan undslippe omprogrammeringsprocessen.
Professor Wolf Reik, en gruppeleder i epigenetikforskningsprogrammet, som for nylig flyttede til at lede Altos Labs Cambridge Institute, sagde: "Dette arbejde har meget spændende implikationer.
"Vi kan muligvis identificere gener, der forynges uden omprogrammering og målrette dem for at reducere virkningerne af aldring.
"Denne tilgang lover værdifulde opdagelser, der kan åbne fantastiske terapeutiske horisonter."
Professor Reik fortæller BBC at betegnelserne ungdomseliksir eller anti-aging pille ikke er helt absurde.
"Teknikken er blevet brugt på genetisk modificerede mus, og der er nogle tegn på foryngelse," sagde han.
"En undersøgelse viste tegn på en forynget bugspytkirtel, som er interessant for dens potentiale til at bekæmpe diabetes."

 Suche
Suche
 Mein Konto
Mein Konto