Het is al eeuwenlang de droom van vrouwen – en mannen. Nu zeggen wetenschappers dat ze een manier hebben gevonden om het verouderingsproces in de menselijke huid om te keren.
Onderzoekers in Cambridge onthullen dat ze huidcellen van mensen van 38 en 53 jaar oud hebben geherprogrammeerd om ze 30 jaar “jonger” te maken.
De procedure draait de verouderingsklok verder terug dan eerdere herprogrammeringsprocedures zonder de cellen te beschadigen.
Onderzoekers zeggen dat ze zelfs gedeeltelijk functies kunnen herstellen die verloren gingen in oudere cellen.
Hoewel het onderzoek zich nog in de beginfase bevindt, kunnen de bevindingen uiteindelijk een revolutie teweegbrengen in de regeneratieve geneeskunde, vooral als ze kunnen worden gerepliceerd in andere celtypen en andere weefsels in het lichaam, beweren de onderzoekers.
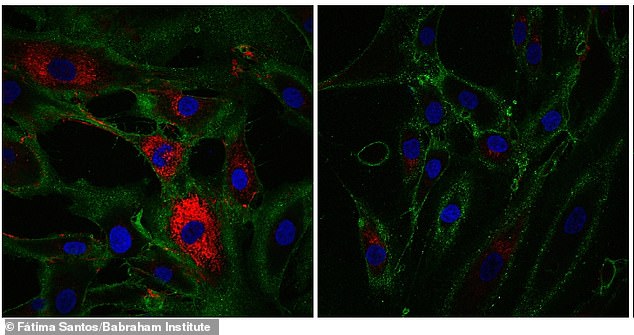
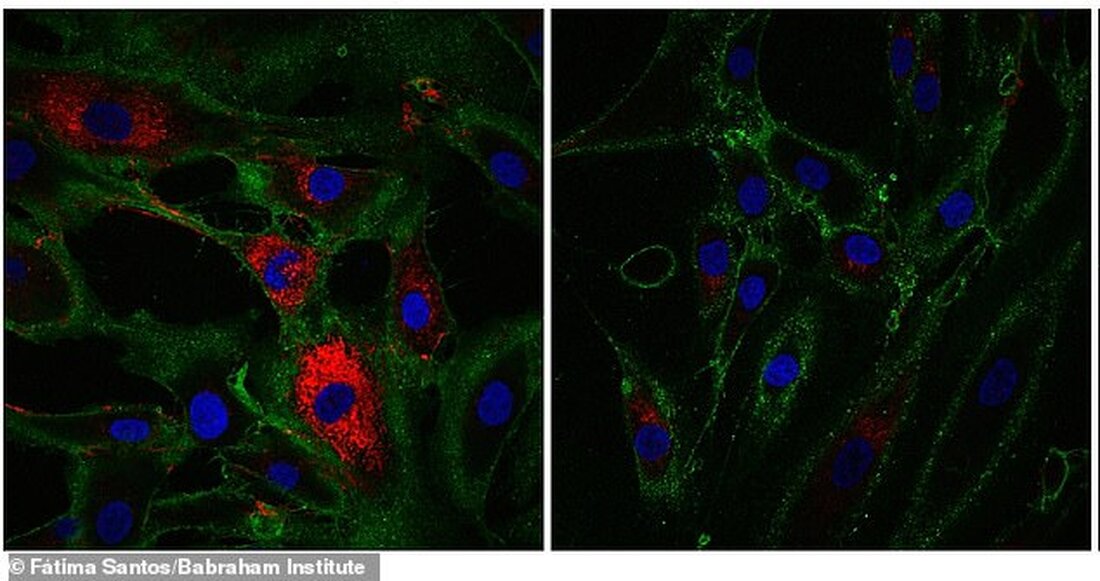
In experimenten hadden verouderende cellen markers teruggevonden die kenmerkend zijn voor huidcellen die collageen produceren, een molecuul dat wordt aangetroffen in botten, huidpezen en ligamenten en dat helpt weefsel te structureren en wonden te genezen. Hier toont rood de productie van collageen door huidcellen die fibroblasten worden genoemd
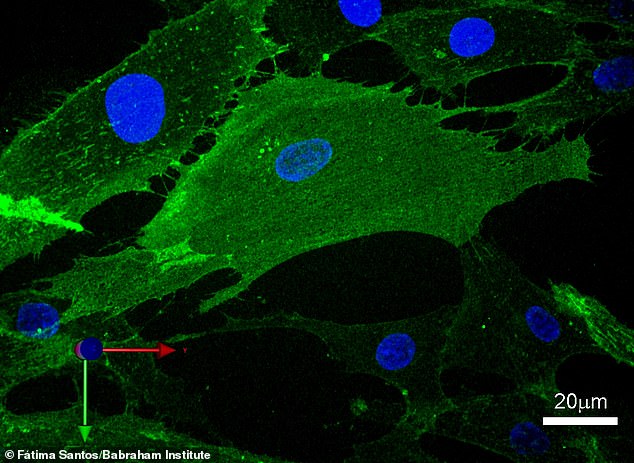
Cellen veranderen tijdelijk van vorm tijdens tijdelijke herprogrammering. Deze afbeelding toont een enkele cel met fibroblast-oppervlaktemarkeringen in groen
Verouderende cellen in experimentenHet begon meer op huidcellen te lijken, fibroblasten genaamd, die collageen produceren, een eiwit dat het lichaam bij elkaar houdt en sterk houdt.
Het aantal fibroblasten in de menselijke huid neemt geleidelijk af met de leeftijd. Deze cellen krimpen ook naarmate we ouder worden.
De nieuwe bevindingen zouden kunnen leiden tot een gerichte aanpak van de behandeling van veroudering die de regeneratieve geneeskunde zou kunnen ‘revolutioneren’, zeggen onderzoekers.
Het nieuwe onderzoek werd uitgevoerd aan het Babraham Institute, een onderzoeksinstituut voor levenswetenschappen in Cambridge, en gepubliceerd in het tijdschrift eLife.
“Onze resultaten vertegenwoordigen een grote vooruitgang in ons begrip van celherprogrammering”, zegt Dr. Diljeet Gill van het Babraham Institute.
“We hebben bewezen dat cellen verjongd kunnen worden zonder hun functie te verliezen en dat verjonging erop gericht is een bepaalde functie van oude cellen te herstellen.
“Het feit dat we ook een omkering van verouderingsindicatoren in ziektegerelateerde genen zagen, is bijzonder veelbelovend voor de toekomst van dit werk.”
Met het ouder worden neemt de functionaliteit van de cellen af en wordt het genoom – hun DNA-blauwdruk – verrijkt met tekenen van veroudering.
Regeneratieve biologie heeft tot doel cellen, zelfs oude, te repareren of te vervangen.
Een van de belangrijkste instrumenten in de regeneratieve biologie is ons vermogen om “geïnduceerde” stamcellen te creëren.
Dit proces verwijdert echter in wezen de cellen van hun functie, waardoor ze het potentieel hebben om elk celtype te worden.
Het werk komt oorspronkelijk voort uit werk aan het Roslin Institute in Edinburgh in de jaren negentig om een borstcel van een zesjarig schaap om te zetten in een embryo.
Dit project leidde op beroemde wijze tot de creatie van Dolly het schaap, het eerste zoogdier dat werd gekloond uit een volwassen somatische cel.
Dolly's creatie toonde aan dat genen in de kern van een volwassen cel nog steeds in staat zijn terug te keren naar een embryonale totipotente toestand - wat betekent dat de cel zich kan delen om alle verschillende cellen van een dier te produceren.

Dolly het schaap (foto) werd in juli 1996 geboren in het Roslin Institute in Edinburgh. Het werd gekweekt uit een borstcel van een zesjarig schaap
Dit maakte de weg vrij voor de Nobelprijswinnende wetenschapper Dr. Shinya Yamanaka, die in 2007 de eerste wetenschapper werd die normale cellen met een specifieke functie omzette in stamcellen die het bijzondere vermogen hebben zich tot elk celtype te ontwikkelen.
Deze methode, IPS genaamd, duurt ongeveer 50 dagen en maakt gebruik van vier sleutelmoleculen die Yamanaka-transcriptiefactoren worden genoemd: Oct4, Sox2, Klf4 en cMyc.
De nieuwe methode van het Babraham Institute, genaamd Maturation Phase Transient Reprogramming, stelt cellen slechts 13 dagen bloot aan Yamanaka-factoren in plaats van 50 dagen.
Op dat moment waren de cellen nog niet in embryonale stamcellen veranderd, maar werden ze “verjongd” alsof ze 30 jaar jonger waren.
De gedeeltelijk geherprogrammeerde cellen kregen de tijd om onder normale omstandigheden te groeien om te zien of hun specifieke huidcelfunctie terugkeerde.
Uit de genomische analyse bleek dat de cellen markers hadden teruggevonden die kenmerkend zijn voor huidcellen (fibroblasten), wat werd bevestigd door observatie van de collageenproductie in de geherprogrammeerde cellen.
Om aan te tonen dat de cellen verjongd waren, zochten de onderzoekers naar veranderingen in de kenmerken van veroudering.

Het onderzoek omvat zogenaamde Yamanaka-transcriptiefactoren, genoemd naar de Nobelprijswinnende Japanse wetenschapper Dr. Shinya Yamanaka (foto).
De onderzoekers onderzochten verschillende maten van celleeftijd. De eerste is de epigenetische klok, waarbij chemische markeringen in het hele genoom de leeftijd aangeven.
De tweede is het transcriptoom, alle genuitlezingen die door de cel worden geproduceerd.
Door deze twee metingen kwamen de geherprogrammeerde cellen overeen met het profiel van cellen die 30 jaar jonger waren in vergelijking met referentiedatasets, aldus het team.
De techniek kan niet onmiddellijk worden vertaald naar een klinische setting omdat PD het risico op kanker verhoogt.
Voorlopig zijn de volgende onderzoeksstappen het begrijpen van het exacte mechanisme dat deze gedeeltelijke herprogrammering mogelijk maakte, maar uiteindelijk zou het kunnen worden gebruikt voor celtherapieën in situaties waarin de leeftijd van de cellen een verschil maakt, zoals: B. bij huidgenezing door brandwonden.
Potentiële toepassingen van deze techniek zijn afhankelijk van het feit dat de cellen er niet alleen jonger uitzien, maar ook functioneren als jonge cellen.
Fibroblasten produceren collageen, een molecuul dat wordt aangetroffen in botten, huidpezen en ligamenten en dat helpt weefsels te structureren en wonden te genezen.
De verjongde fibroblasten produceerden meer collageeneiwitten vergeleken met controlecellen die het herprogrammeringsproces niet hadden ondergaan, ontdekten onderzoekers van het Babraham Institute.
Fibroblasten verplaatsen zich ook naar gebieden die gerepareerd moeten worden, dus testten de onderzoekers de gedeeltelijk verjongde cellen door een kunstmatige snede te maken in een laag cellen in een schaaltje.
Ze ontdekten dat hun behandelde fibroblasten sneller in de opening terechtkwamen dan oudere cellen - een veelbelovend teken dat er op een dag cellen zouden kunnen worden gecreëerd die beter zijn in het genezen van wonden.
De onderzoekers willen ook kijken of de nieuwe methode werkt op andere weefsels zoals spieren, lever en bloedcellen.
In de toekomst zou dit onderzoek ook andere therapeutische mogelijkheden kunnen openen; De onderzoekers merkten op dat hun methode ook effecten had op andere genen die verband houden met leeftijdsgebonden ziekten en symptomen.
Het APBA2-gen, dat geassocieerd is met de ziekte van Alzheimer, en het MAF-gen, dat een rol speelt bij de ontwikkeling van cataract, vertoonden beide veranderingen in de richting van jeugdige transcriptieniveaus.

De nieuwe bevindingen zouden kunnen leiden tot een gerichte aanpak van de behandeling van veroudering die een revolutie teweeg zou kunnen brengen in de regeneratieve geneeskunde (bestandsfoto)
Het mechanisme achter succesvolle tijdelijke herprogrammering is nog niet volledig begrepen en is het volgende stukje van de puzzel dat moet worden onderzocht.
De onderzoekers speculeren dat belangrijke regio's van het genoom die betrokken zijn bij de vorming van celidentiteit aan het herprogrammeringsproces kunnen ontsnappen.
Professor Wolf Reik, een groepsleider in het epigenetica-onderzoeksprogramma die onlangs de leiding kreeg over het Altos Labs Cambridge Institute, zei: “Dit werk heeft zeer opwindende implicaties.
“Misschien kunnen we genen identificeren die verjongen zonder herprogrammering en hierop richten om de effecten van veroudering te verminderen.
“Deze aanpak belooft waardevolle ontdekkingen die verbazingwekkende therapeutische horizonten kunnen openen.”
Professor Reik vertelt de BBC dat de termen jeugdelixer of antiverouderingspil niet geheel absurd zijn.
“De techniek is gebruikt op genetisch gemodificeerde muizen en er zijn enkele tekenen van verjonging,” zei hij.
“Eén onderzoek toonde tekenen van een verjongde alvleesklier, wat interessant is vanwege zijn potentieel om diabetes te bestrijden.”

 Suche
Suche
 Mein Konto
Mein Konto