Gli scienziati stanno sviluppando organoidi delle ghiandole salivari umane per testare l’infettività della SARS-CoV-2
In un recente studio pubblicato sulla rivista Nature Cell Biology, i ricercatori hanno dimostrato la suscettibilità delle ghiandole salivari alle gravi infezioni da sindrome respiratoria acuta coronavirus-2 (SARS-CoV-2) in vitro utilizzando un modello di coltura organoide. Studio: Gli organoidi della ghiandola salivare derivati dalle cellule staminali pluripotenti indotte dall'uomo modellano l'infezione e la replica di SARS-CoV-2. Credito immagine: NIAID Background Sebbene il sistema respiratorio, compreso il tratto respiratorio superiore (URT) e i polmoni, siano gli obiettivi primari della SARS-CoV-2, vi sono prove crescenti che colpisca più organi. Ad esempio, la mucosa orale e le ghiandole salivari esprimono ampiamente due fattori di ingresso della SARS-CoV-2, l’enzima di conversione dell’angiotensina 2 (ACE2) e la serina proteasi transmembrana 2 (TMPRSS2). Fungono anche da serbatoio per SARS-CoV-2. …
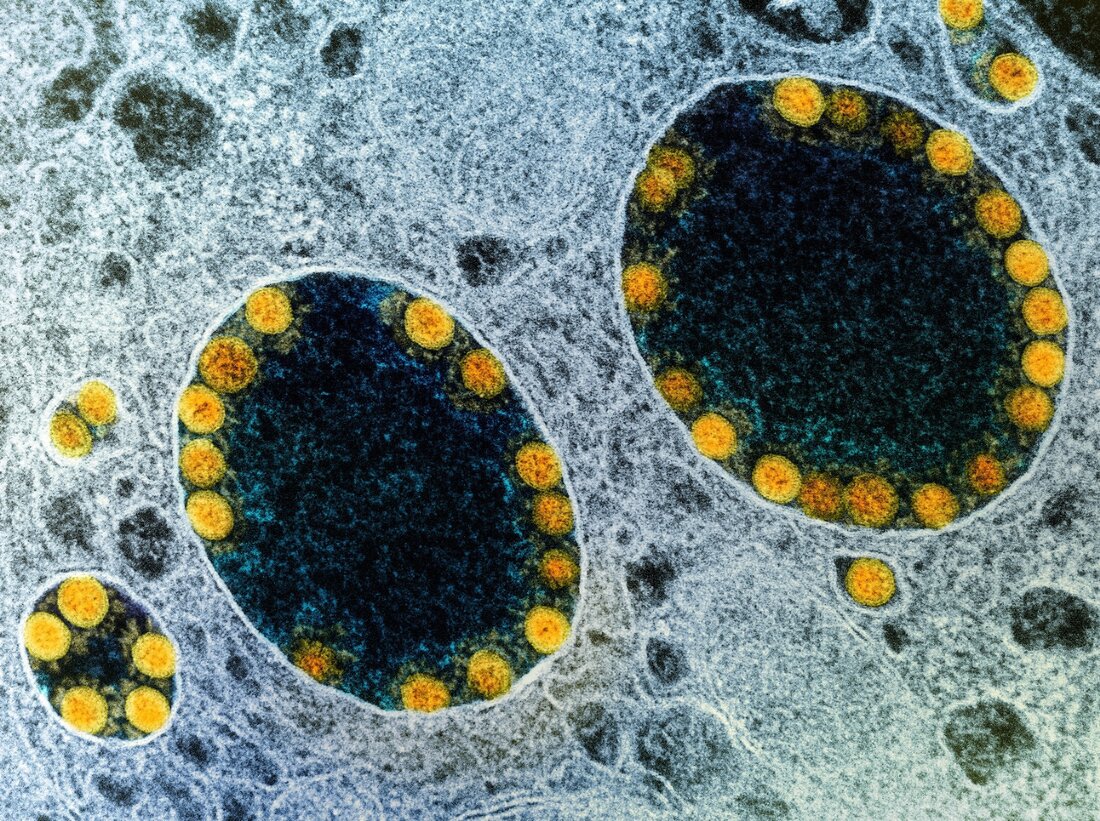
Gli scienziati stanno sviluppando organoidi delle ghiandole salivari umane per testare l’infettività della SARS-CoV-2
In uno studio recentemente pubblicato sulla rivista Biologia cellulare naturale I ricercatori hanno dimostrato in vitro la suscettibilità delle ghiandole salivari all’infezione da sindrome respiratoria acuta grave da coronavirus-2 (SARS-CoV-2) utilizzando un modello di coltura organoide.
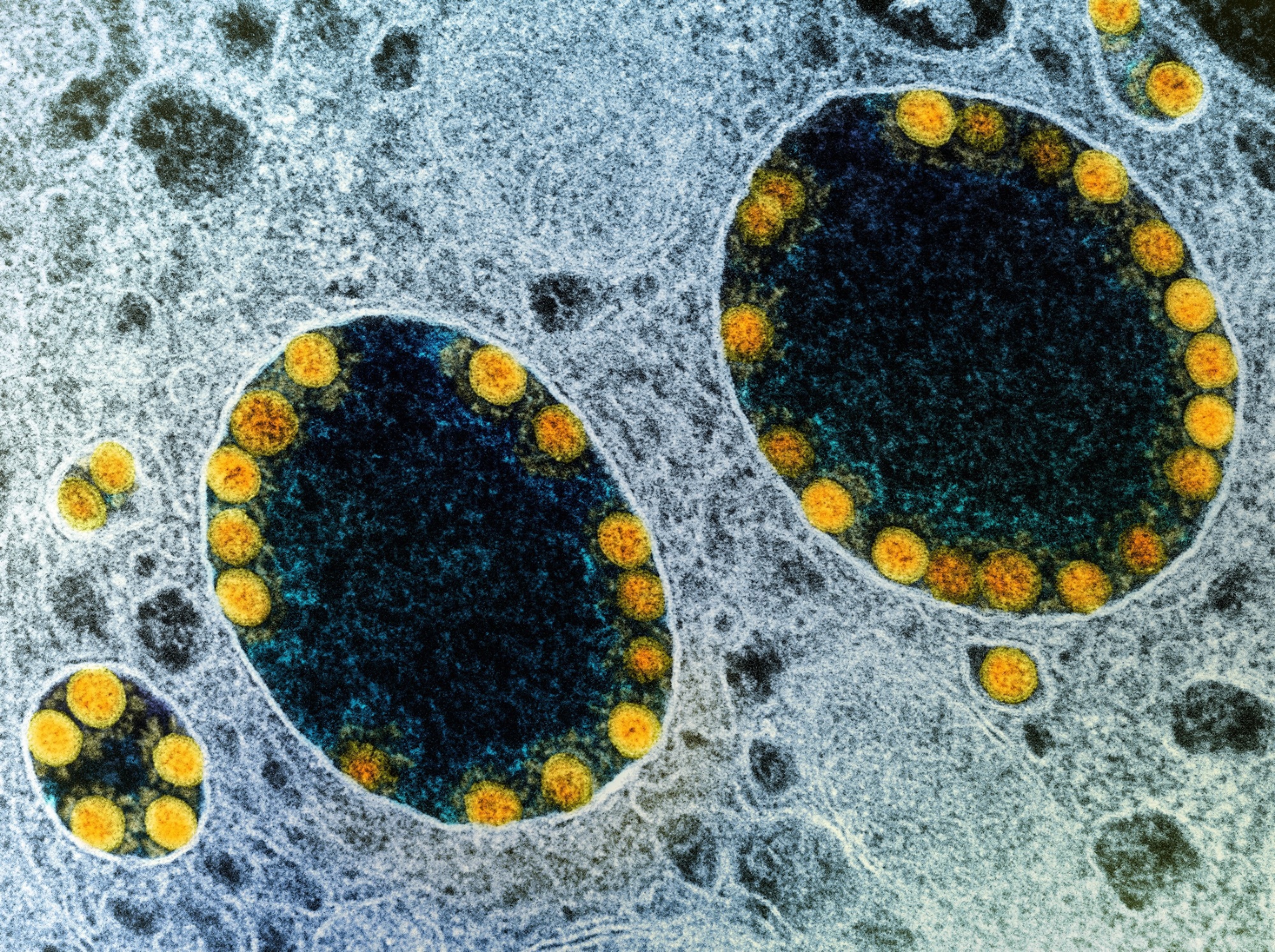
sfondo
Sebbene il sistema respiratorio, compreso il tratto respiratorio superiore (URT) e i polmoni, siano i principali bersagli della SARS-CoV-2, vi sono prove crescenti che colpisca più organi. Ad esempio, la mucosa orale e le ghiandole salivari esprimono ampiamente due fattori di ingresso della SARS-CoV-2, l’enzima di conversione dell’angiotensina 2 (ACE2) e la serina proteasi transmembrana 2 (TMPRSS2). Fungono anche da serbatoio per SARS-CoV-2.
È interessante notare che l’80% delle infezioni da SARS-CoV-2 sono asintomatiche. Inoltre, gli studi hanno riferito che la SARS-CoV-2 prende di mira le ghiandole salivari umane e che i virioni infettivi provenienti dalla saliva di individui asintomatici contribuiscono a un’ulteriore trasmissione del virus.
A causa della capacità di SARS-CoV-2 di infettare più tipi di organoidi, un modello di coltura di organoidi può rivelarsi adatto per rilevare l’infezione da SARS-CoV-2 nelle ghiandole salivari (in vitro). Tuttavia, a causa della mancanza di modelli in vitro adeguati, gli studi non sono riusciti a chiarire i meccanismi alla base dell’infezione e della replicazione del SARS-CoV-2 nelle ghiandole salivari e della successiva secrezione nella saliva.
A proposito dello studio
Nel presente studio, i ricercatori hanno generato organoidi funzionali delle ghiandole salivari da cellule staminali pluripotenti indotte umane (hiPSC) con caratteristiche morfologiche e funzioni fisiologiche simili (in vivo) alle ghiandole salivari umane. Inoltre, questi organoidi avevano linee cellulari specifiche delle ghiandole salivari.
Il team ha eseguito il sequenziamento dell’acido ribonucleico unicellulare (scRNA-seq) delle cellule hiSG il giorno 80 utilizzando la piattaforma 10X Genomics. Inoltre, hanno isolato gli organoidi il giorno 60 e li hanno coltivati con il fattore di crescita dei fibroblasti (FGF) 7 e 10 fino al giorno 80 per caratterizzare le strutture di ramificazione osservate.
Il gene del fattore di trascrizione SRY-box 9 (SOX9) regola lo sviluppo delle ghiandole salivari nei topi e nell'uomo. In sua assenza, le ghiandole salivari non possono subire morfogenesi ramificata. Pertanto, i ricercatori hanno soppresso SOX9 durante l'induzione di hiSG per scoprire se gli hiSG ricapitolavano il processo di sviluppo mediato da SOX9.
Risultati dello studio
Le ghiandole salivari indotte dall'uomo (hiSG) avevano proprietà simili alle ghiandole salivari embrionali, comprese caratteristiche morfologiche, espressione di marcatori proteici e caratteristiche di espressione genica. Coerentemente con gli studi in vivo condotti sui topi, il knockdown di SOX9 ha inibito la formazione di rami nelle hiPSC, suggerendo che questo gene è fondamentale per lo sviluppo delle ghiandole salivari umane. Pertanto, questo modello di studio potrebbe sostituire i modelli animali utilizzati per studiare lo sviluppo delle ghiandole salivari umane.
Gli hiSG imitavano morfologicamente e funzionalmente le ghiandole salivari naturali. Il clustering imparziale scRNA-seq ha identificato sei gruppi cellulari principali che sono ulteriormente divisibili in sottotipi cellulari. La piccola popolazione mesenchimale negli HiSG non mostrava caratteristiche del mesenchima delle ghiandole salivari. Al contrario, il gruppo di cellule epiteliali era costituito da cinque gruppi cellulari: cellule acinose, basali, duttali, mioepiteliali e cellule a ciclo attivo. Gli hiSG comprendevano lignaggi indipendenti di cellule mioepiteliali basali del lignaggio duttale-acinare e l'analisi pseudotime ha dimostrato le differenze tra questi due lignaggi cellulari.
La funzione di base delle ghiandole salivari è quella di secernere il fluido indotto dall'acetilcolina attraverso le vie del recettore muscarinico dell'acetilcolina. Negli hiSG, il trattamento con carbacolo, un agonista del recettore muscarinico dell’acetilcolina, ha determinato un aumento transitorio e dose-dipendente dei livelli di calcio intracellulare. Inoltre, gli hiSG trapiantati ortotopicamente hanno mostrato nel tempo il fenotipo delle ghiandole salivari mature trapiantate in un sito ricevente nei topi.
Le analisi scRNA-seq e immunofluorescenza hanno anche mostrato che le cellule duttali all'interno degli hiSG esprimevano abbondantemente ACE2 e TMPRSS2, simili alle normali ghiandole salivari. Il metodo di immunocolorazione ha rivelato che sebbene le cellule duttali sul lato apicale degli hiSG esprimessero fortemente ACE2, le cellule duttali e le cellule acinose esprimevano TMPRSS2. Al contatto con SARS-CoV-2, gli hiSG si sono infettati e hanno mostrato la replicazione di SARS-CoV-2 entro 24 ore dall’infezione. Gli autori hanno anche scoperto la nucleoproteina SARS-CoV-2 nelle cellule duttali infette. Di conseguenza, il test di coltura di tessuto infettivo medio (TCID50) ha mostrato virus infettivi negli hiSG che hanno raggiunto il picco a 24 ore ma sono diminuiti successivamente.
Conclusioni
In effetti, gli hiSG sviluppati nel presente studio potrebbero fungere da modello prezioso per la riproduzione di popolazioni cellulari eterogenee nelle ghiandole salivari umane. Inoltre, gli hiSG potrebbero supportare l’analisi funzionale dei geni durante lo sviluppo e fungere da strumento promettente per studiare le infezioni da SARS-CoV-2 nelle ghiandole salivari a livello molecolare. Inoltre, i ricercatori hanno dimostrato che gli hiSG presentavano diversi vantaggi rispetto agli organoidi derivati da cellule progenitrici staminali dei tessuti delle ghiandole salivari umane adulte. Ad esempio, potrebbero essere facilmente modificati geneticamente utilizzando lo strumento di editing genetico CRISPR (brevi ripetizioni palindromiche raggruppate regolarmente interspaziate) e la proteina 9 associata a CRISPR (Cas9) ed erano relativamente facili da coltivare.
Riferimento:
- Tanaka, J., Senpuku, H., Ogawa, M. et al. Vom Menschen induzierte pluripotente, aus Stammzellen gewonnene Speicheldrüsenorganoide modellieren die SARS-CoV-2-Infektion und -Replikation. Nat Cell Biol (2022). https://doi.org/10.1038/s41556-022-01007-6, https://www.nature.com/articles/s41556-022-01007-6#Sec7

 Suche
Suche
 Mein Konto
Mein Konto
