科学家正在开发人类唾液腺类器官来测试 SARS-CoV-2 的传染性
在《自然细胞生物学》杂志最近发表的一项研究中,研究人员使用类器官培养模型在体外证明了唾液腺对急性呼吸综合征冠状病毒-2(SARS-CoV-2)严重感染的易感性。研究:人类诱导的多能干细胞来源的唾液腺类器官模拟 SARS-CoV-2 感染和复制。图片来源:NIAID 背景 尽管包括上呼吸道 (URT) 和肺部在内的呼吸系统是 SARS-CoV-2 的主要目标,但越来越多的证据表明它会影响多个器官。例如,口腔粘膜和唾液腺广泛表达两种 SARS-CoV-2 进入因子:血管紧张素转换酶 2 (ACE2) 和跨膜丝氨酸蛋白酶 2 (TMPRSS2)。它们还充当 SARS-CoV-2 的储存库。 ……
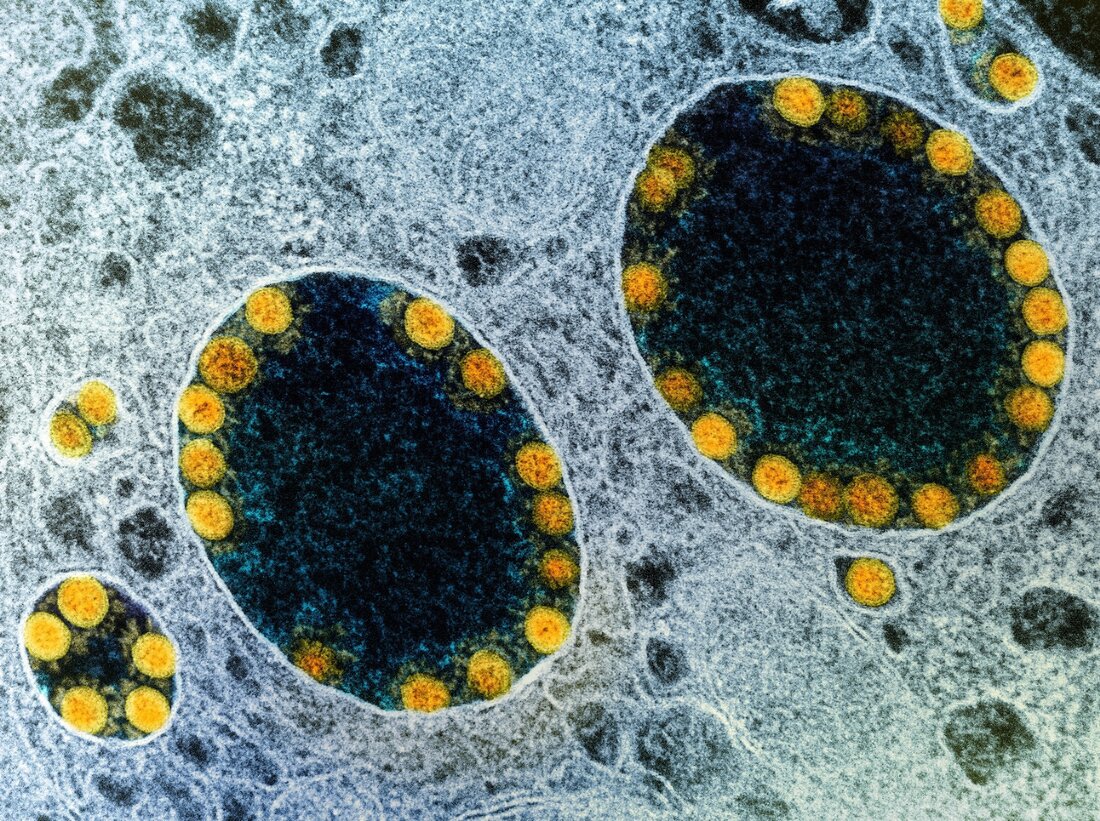
科学家正在开发人类唾液腺类器官来测试 SARS-CoV-2 的传染性
在最近发表在该杂志上的一项研究中 天然细胞生物学 研究人员使用类器官培养模型在体外证明了唾液腺对严重急性呼吸综合征冠状病毒-2 (SARS-CoV-2) 感染的易感性。
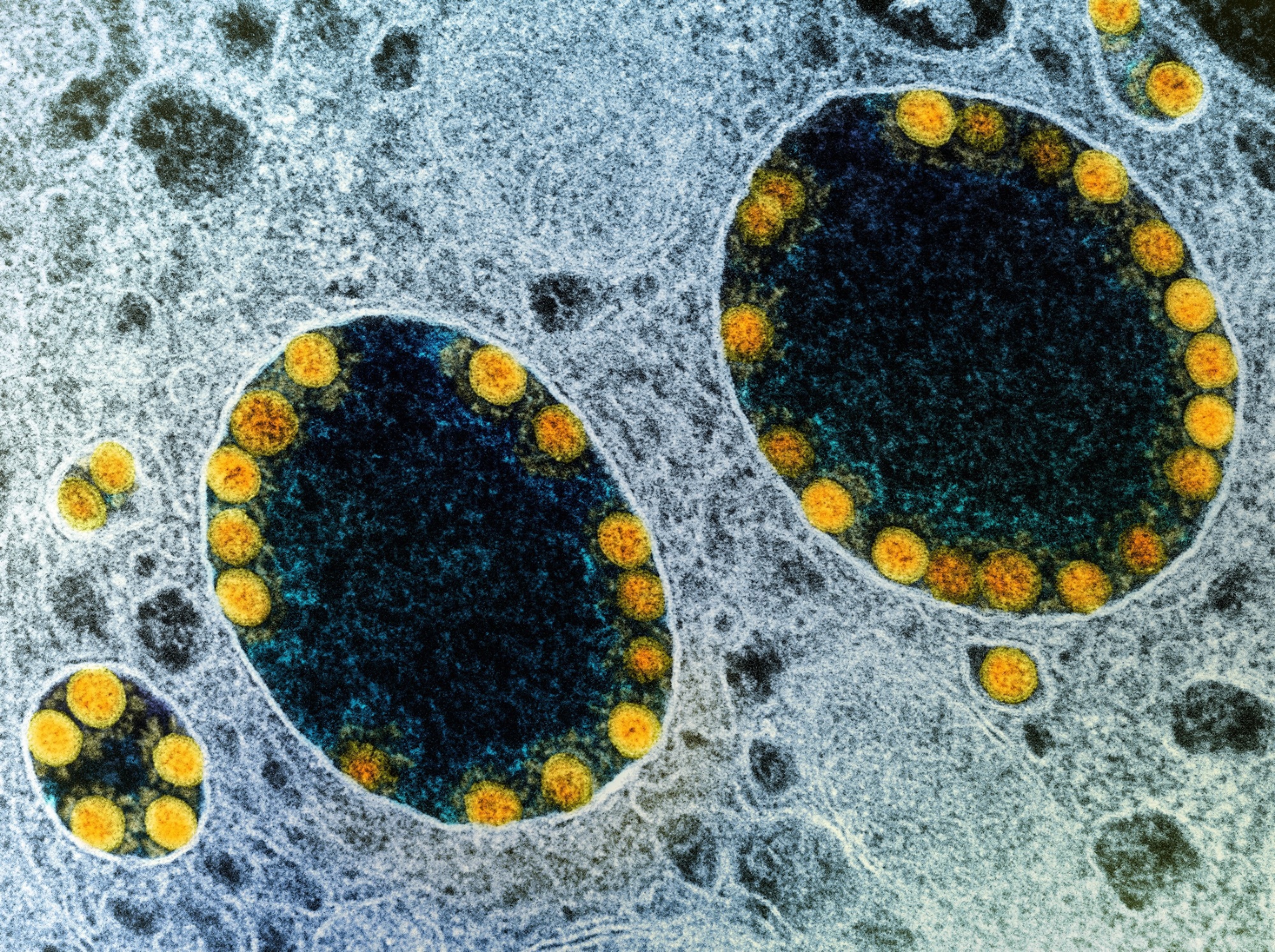
背景
尽管包括上呼吸道 (URT) 和肺部在内的呼吸系统是 SARS-CoV-2 的主要目标,但越来越多的证据表明它会影响多个器官。 例如,口腔粘膜和唾液腺广泛表达两种 SARS-CoV-2 进入因子:血管紧张素转换酶 2 (ACE2) 和跨膜丝氨酸蛋白酶 2 (TMPRSS2)。 它们还充当 SARS-CoV-2 的储存库。
有趣的是,80% 的 SARS-CoV-2 感染者是无症状的。 此外,研究报告称,SARS-CoV-2 以人类唾液腺为目标,无症状个体唾液中的传染性病毒粒子有助于病毒进一步传播。
由于 SARS-CoV-2 能够感染多种类型的类器官,类器官培养模型可能适合检测唾液腺中 SARS-CoV-2 的感染(体外)。 然而,由于缺乏合适的体外模型,研究未能阐明SARS-CoV-2在唾液腺中感染和复制以及随后分泌到唾液中的机制。
关于该研究
在本研究中,研究人员从人类诱导多能干细胞(hiPSC)中生成了功能性唾液腺类器官,其形态特征和生理功能(体内)与人类唾液腺相似。 此外,这些类器官具有唾液腺特异性细胞系。
该团队在第 80 天使用 10X Genomics 平台对 hiSG 细胞进行了单细胞核糖核酸测序 (scRNA-seq)。 此外,他们在第 60 天分离了类器官,并将其与成纤维细胞生长因子 (FGF) 7 和 10 一起培养直至第 80 天,以表征观察到的分支结构。
SRY-box 转录因子 9 (SOX9) 基因调节小鼠和人类的唾液腺发育。 如果没有它,唾液腺就不能进行分支形态发生。 因此,研究人员在 hiSG 诱导过程中抑制 SOX9,以查明 hiSG 是否重现了 SOX9 介导的发育过程。
研究结果
人诱导唾液腺(hiSG)与胚胎唾液腺具有相似的特性,包括形态特征、蛋白质标记表达和基因表达特征。 与在小鼠中进行的体内研究一致,SOX9 敲除抑制了 hiPSC 中的分支形成,表明该基因对于人类唾液腺发育至关重要。 因此,该研究模型可以取代用于研究人类唾液腺发育的动物模型。
hiSG 在形态和功能上模仿天然唾液腺。 无偏 scRNA-seq 聚类确定了六个主要细胞群,这些细胞群可进一步分为细胞亚型。 HiSG 中的少量间充质群体没有表现出唾液腺间充质的特征。 相反,上皮细胞群由五个细胞群组成:腺泡细胞、基底细胞、导管细胞、肌上皮细胞和活跃循环细胞。 hiSG 包含来自导管腺泡谱系的独立基底肌上皮细胞谱系,伪时间分析证明了这两个细胞谱系之间的差异。
唾液腺的基本功能是通过毒蕈碱乙酰胆碱受体途径分泌乙酰胆碱诱导的液体。 在 hiSG 中,用卡巴胆碱(一种毒蕈碱乙酰胆碱受体激动剂)治疗会导致细胞内钙水平出现短暂且剂量依赖性的增加。 此外,随着时间的推移,原位移植的 hiSG 表现出移植到小鼠受体部位的成熟唾液腺的表型。
scRNA-seq 和免疫荧光分析还表明 hiSG 内的导管细胞大量表达 ACE2 和 TMPRSS2,与正常唾液腺相似。 免疫染色方法显示,虽然hiSGs顶端的导管细胞强烈表达ACE2,但导管细胞和腺泡细胞表达TMPRSS2。 接触 SARS-CoV-2 后,hiSG 被感染,并在感染后 24 小时内出现 SARS-CoV-2 复制。 作者还在受感染的导管细胞中发现了 SARS-CoV-2 核蛋白。 因此,培养基感染性组织培养测定(TCID50)显示 hiSG 中的感染性病毒在 24 小时达到峰值,但随后下降。
结论
事实上,当前研究中开发的 hiSG 可以作为人类唾液腺异质细胞群繁殖的有价值的模型。 此外,hiSG 可以支持发育过程中基因的功能分析,并作为在分子水平上研究唾液腺 SARS-CoV-2 感染的有前途的工具。 此外,研究人员还表明,与源自成人唾液腺组织干祖细胞的类器官相比,hiSG 具有多种优势。 例如,它们可以使用基因编辑工具 CRISPR(成簇规则间隔短回文重复)和 CRISPR 相关蛋白 9 (Cas9) 轻松进行基因改造,并且相对容易培养。
参考:
- Tanaka, J., Senpuku, H., Ogawa, M. et al. Vom Menschen induzierte pluripotente, aus Stammzellen gewonnene Speicheldrüsenorganoide modellieren die SARS-CoV-2-Infektion und -Replikation. Nat Cell Biol (2022). https://doi.org/10.1038/s41556-022-01007-6, https://www.nature.com/articles/s41556-022-01007-6#Sec7

 Suche
Suche
 Mein Konto
Mein Konto
