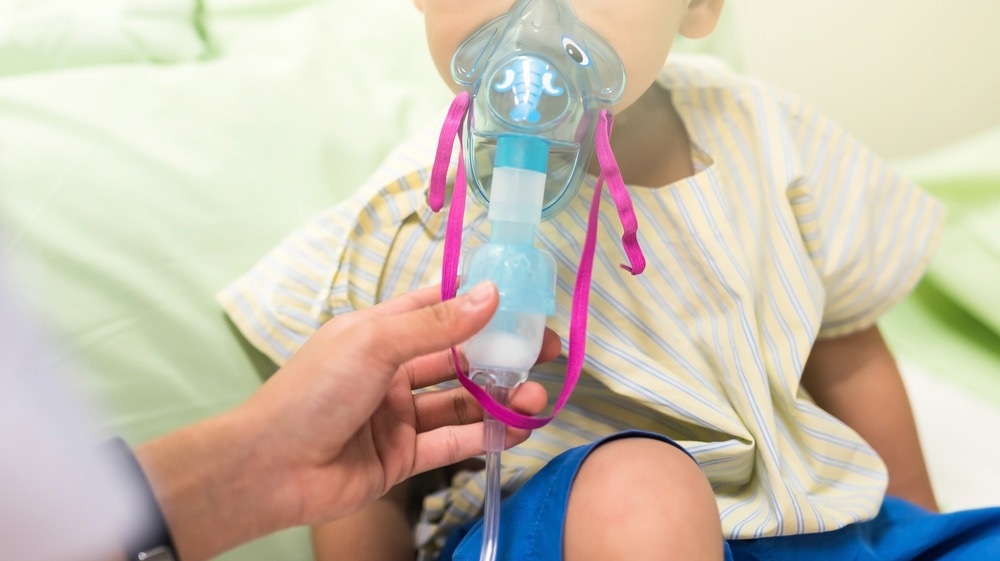
Le vaccin maternel contre le VRS de Pfizer protège les nouveau-nés des maladies graves
Le 1er novembre 2022, Pfizer a annoncé que son vaccin contre le virus respiratoire syncytial maternel (VRS) était efficace à près de 82 % pour protéger les nourrissons contre les maladies graves causées par le VRS au cours des 90 premiers jours de leur vie. En outre, le vaccin s’est avéré efficace à 69,4 % pour prévenir les maladies graves à VRS au cours des six premiers mois de la vie. Apprendre : Pfizer annonce des données positives d'essai mondial de phase 3 sur l'immunisation maternelle pour son candidat vaccin bivalent contre le virus respiratoire syncytial (RSV). Crédit image : Blanscape / Shutterstock.com Qu'est-ce que le RSV ? Le VRS est la cause la plus fréquente d’infections respiratoires chez les enfants de deux ans et moins. En fait, certaines estimations suggèrent que...
Le vaccin maternel contre le VRS de Pfizer protège les nouveau-nés des maladies graves
Le 1er novembre 2022, Pfizer a annoncé que son vaccin contre le virus respiratoire syncytial maternel (VRS) était efficace à près de 82 % pour protéger les nourrissons contre les maladies graves causées par le VRS au cours des 90 premiers jours de leur vie. En outre, le vaccin s’est avéré efficace à 69,4 % pour prévenir les maladies graves à VRS au cours des six premiers mois de la vie.
Apprendre: Pfizer annonce des données positives d'essai mondial de phase 3 sur l'immunisation maternelle pour son candidat vaccin bivalent contre le virus respiratoire syncytial (RSV).Crédit photo : Blanscape / Shutterstock.com
Qu’est-ce que le VRS ?
Le VRS est la cause la plus fréquente d’infections respiratoires chez les enfants de deux ans et moins. En fait, certaines estimations suggèrent que plus de 60 % des enfants seront infectés par le VRS avant l’âge d’un an, et que presque tous les enfants seront susceptibles d’être infectés avant l’âge de deux ans.
L’infection par le VRS provoque généralement des symptômes semblables à ceux du rhume, tels qu’un écoulement nasal, une diminution de l’appétit, de la toux, des éternuements, de la fièvre et une respiration sifflante. Néanmoins, le RSV peut provoquer une maladie grave chez un nombre important d'enfants de moins d'un an et constitue donc la principale cause de décès par infections respiratoires dans cette population de patients.
Plusieurs facteurs peuvent augmenter le risque de maladie grave à VRS chez un enfant, notamment le fait d'avoir moins d'un an avant ou pendant le pic d'incidence du virus, ainsi que la prématurité, un faible poids à la naissance et la présence de comorbidités telles qu'une cardiopathie congénitale, une maladie respiratoire chronique et une immunodéficience. En outre, les enfants ayant un frère ou une sœur plus âgé et ceux qui sont exposés à la fumée de cigarette et ne sont pas allaités courent également un risque plus élevé d’infection grave par le VRS.
Chaque année, nous constatons des niveaux élevés de cas de VRS chez les bébés aux États-Unis, certaines régions signalant cette année des taux d’hospitalisation plus élevés que la normale.
Le vaccin RSVpreF de Pfizer
Il n’existe toujours pas de traitement spécifique contre l’infection par le RSV ; Par conséquent, les enfants infectés par ce virus, y compris ceux hospitalisés pour une maladie grave, reçoivent généralement un traitement symptomatique jusqu'à ce que l'infection finisse par disparaître de leur système. Le manque de traitements préventifs et antiviraux contre le VRS a conduit Pfizer à développer et à tester l’efficacité d’un candidat vaccin bivalent par perfusion contre le VRS, connu sous le nom de RSVpreF ou PF-06928316.
Breath Biopsy® : Le manuel complet eBook
Introduction à la biopsie respiratoire, y compris les biomarqueurs, la technologie, les applications et les études de cas. Téléchargez une copie gratuite
Des recherches antérieures menées aux National Institutes of Health (NIH) des États-Unis ont fourni des informations détaillées sur la structure cristalline de la prefusion-F, une forme importante de la protéine de fusion virale du RSV (F) responsable de son entrée dans les cellules hôtes. De plus, il a été démontré que les anticorps spécifiques de la préfusion F préviennent efficacement l’apparition d’une infection par le RSV.
Ces informations ont ensuite été utilisées pour soutenir le développement de RSVpreF, un candidat vaccin expérimental contre le RSV contenant des quantités égales de préfusion F recombinée de RSV provenant des sous-groupes A et B.
Résultats des essais cliniques
RSVpreF a été évalué cliniquement dans deux études, dont l'étude d'efficacité du vaccin contre le VRS iNolder Adults Immunized against RSV Disease (RENOIR) et l'étude MATernal Immunization Study for Safety and Efficacy (MATISSE).
Le Etude MATISSE est un essai clinique de phase III, randomisé, en double aveugle et contrôlé par placebo, évaluant l'innocuité, l'efficacité et l'immunogénicité du RSVpreF. À cette fin, environ 7 400 femmes enceintes à la fin du deuxième ou au troisième trimestre de leur grossesse ont été inscrites à l'étude pour recevoir soit une dose unique du RSVpreF de Pfizer, soit le vaccin placebo.
Les nourrissons nés de mères ayant reçu l’un ou l’autre vaccin ont été suivis pendant au moins un an pour déterminer l’innocuité et l’efficacité du vaccin. De plus, 50 % de ces nourrissons ont été suivis pendant deux ans.
Une efficacité vaccinale de 81,8 % dans la prévention des maladies graves des voies respiratoires inférieures (IVRI) a été rapportée au cours des 90 premiers jours de la vie. Ce niveau élevé d'efficacité contre les maladies graves a été maintenu chez 69,4 % des nourrissons jusqu'à l'âge de six mois.
En plus de la protection contre les IVRI graves, Pfizer rapporte que le vaccin protège contre les LRTI non graves médicalement prises en charge chez 57,1 % et 51,3 % des nourrissons au cours des 90 premiers jours et des six premiers mois de la vie, respectivement.
"Un vaccin maternel très efficace qui peut aider à protéger les nourrissons dès la naissance pourrait réduire considérablement le fardeau du VRS grave chez les nouveau-nés jusqu'à l'âge de six mois."
Perspectives d'avenir
Sur la base des résultats prometteurs de l’essai MATISSE, Pfizer a l’intention de soumettre une demande de licence de produit biologique (BLA) à la Food and Drug Administration (FDA) des États-Unis d’ici la fin de cette année. Bien qu'aucun participant supplémentaire ne soit inscrit à l'essai MATISSE, Pfizer continuera de surveiller les nourrissons nés de mères vaccinées.
Références :
- Pfizer gibt positive Top-Line-Daten der globalen Phase-3-Maternal-Immunisierungsstudie für seinen bivalenten Respiratory-Syncytial-Virus (RSV)-Impfstoffkandidaten bekannt [Online]. Verfügbar ab: https://www.pfizer.com/news/press-release/press-release-detail/pfizer-announces-positive-top-line-data-phase-3-global.
- Azzari, C., Baraldi, E., Bonanni, P., et al. (2021). Epidemiologie und Prävention von Respiratory-Syncytial-Virus-Infektionen bei Kindern in Italien. Italienisches Journal für Pädiatrie 47(198). doi:10.1186/s13052-021-01148-8.
- Die MATISSE-Mütterimpfstoffstudie – https://rsvvaccinestudy.com/en-us/rsv-vaccine-study.html
.

 Suche
Suche
 Mein Konto
Mein Konto