استكشاف أهداف علاجية جديدة ومؤشرات حيوية للأمراض التنكسية العصبية
رؤى من الصناعة شبنا ماسي، مديرة المنتجات المساعدة في شركة Sino Biological US Inc. في هذه المقابلة، تحدثت الدكتورة شبنا ماسي عن الأمراض التنكسية العصبية مثل مرض الزهايمر، ومرض باركنسون، ومرض هنتنغتون والمزيد. كما أنها تناقش وتبحث في الأهداف العلاجية والمؤشرات الحيوية الجديدة لهذه الأمراض. ما هو مقدار المعلومات المعروفة عن مسببات الأمراض التنكسية العصبية والتسبب فيها؟ أدت زيادة متوسط العمر المتوقع إلى أن تصبح الأمراض التنكسية العصبية التقدمية بصمت ذات أهمية متزايدة في جميع أنحاء العالم. تعزى التأثيرات المشتركة للانحرافات الوراثية والعوامل البيئية والعمر بشكل أساسي إلى حدوث أمراض التنكس العصبي مثل مرض الزهايمر (AD)، ومرض باركنسون (PD)، ومرض هنتنغتون (HD) والتصلب الجانبي الضموري (ALS). الخسارة التدريجية..
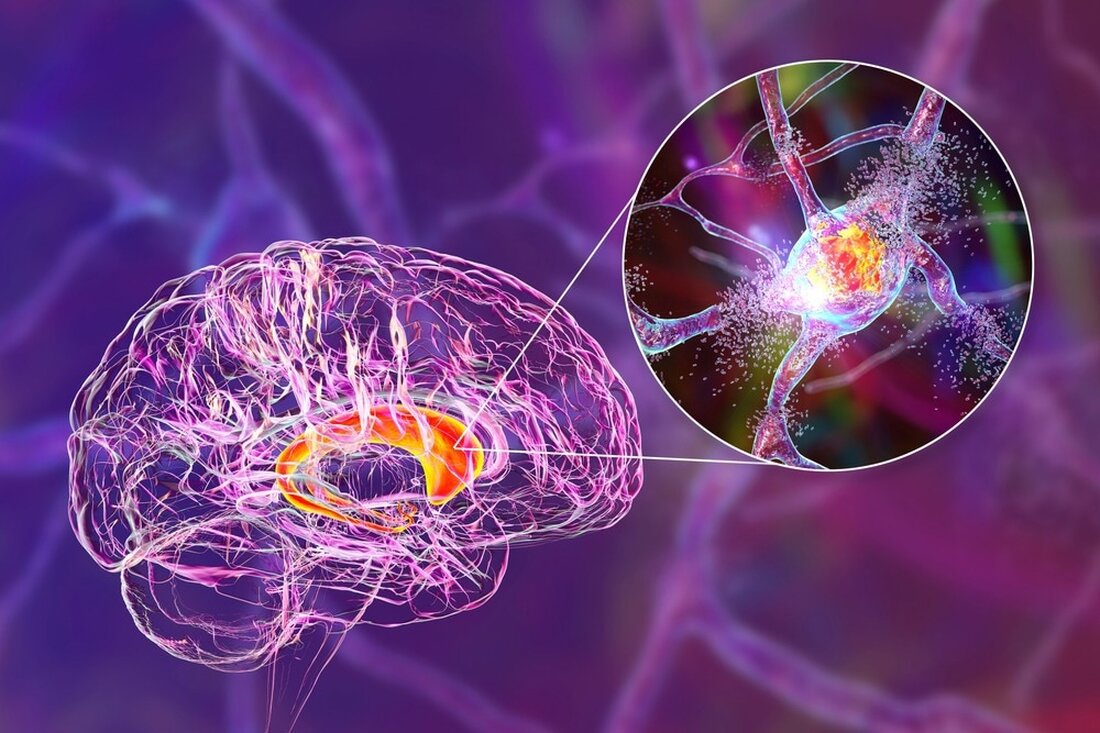
استكشاف أهداف علاجية جديدة ومؤشرات حيوية للأمراض التنكسية العصبية

في هذه المقابلة تتحدث الدكتورة شبنا ماسي عن الأمراض التنكسية العصبية مثل مرض الزهايمر ومرض باركنسون ومرض هنتنغتون وغيرها. كما أنها تناقش وتبحث في الأهداف العلاجية والمؤشرات الحيوية الجديدة لهذه الأمراض.
ما هو مقدار المعلومات المعروفة عن مسببات الأمراض التنكسية العصبية والتسبب فيها؟
أدت زيادة متوسط العمر المتوقع إلى أن تصبح الأمراض التنكسية العصبية التقدمية بصمت ذات أهمية متزايدة في جميع أنحاء العالم.
تعزى التأثيرات المشتركة للانحرافات الوراثية والعوامل البيئية والعمر بشكل أساسي إلى حدوث أمراض التنكس العصبي مثل مرض الزهايمر (AD)، ومرض باركنسون (PD)، ومرض هنتنغتون (HD) والتصلب الجانبي الضموري (ALS).
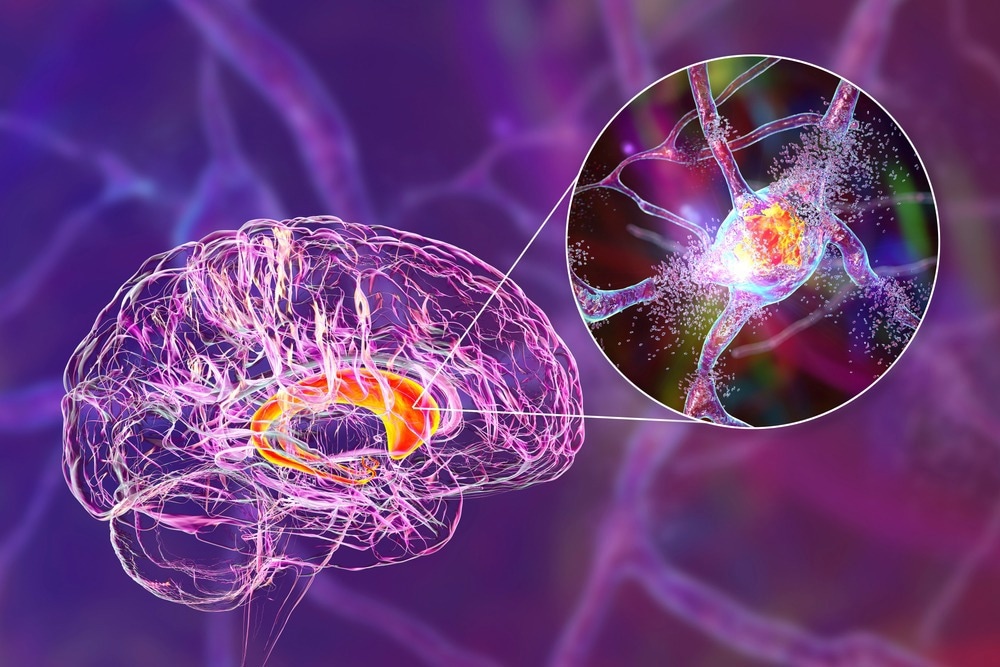
إن الفقدان التدريجي للخلايا العصبية، وخلل الخلايا الدبقية، واختلال الوصلات المتشابكة في الدماغ والحبل الشوكي، كلها عوامل تميز هذه الأمراض من الناحية المرضية.
تقترح بعض وجهات النظر المسببة الجديدة المتغيرة للنموذج أن أمراض القلب والأوعية الدموية هي أساس الاضطرابات الاستتبابية للبروتينات المختلفة التي تضعف الوظيفة الإدراكية.
هناك أيضًا دراسات تسلط الضوء على الوظائف المناعية لمحور الأمعاء والدماغ. مطلوب نهج متكامل ومبتكر لدمج هذه الآراء في وجهات النظر والأبحاث التقليدية والكلاسيكية المسببة للأمراض الأمراض التنكسية العصبية.
مصدر الصورة: كاترينا كون/Shutterstock.com
ما هي الأهداف العلاجية الشائعة في الأمراض التنكسية العصبية؟ ما هي مراحل التطور التي هم فيها؟
يتم تحديد الأمراض التنكسية العصبية بناءً على ارتباط البروتينات السامة المطابقة بشكل غير طبيعي مثل اعتلالات التاو، واعتلالات α-synucleinopathies، واعتلالات بروتينات TDP-43، واعتلالات بروتينات FUS/FET، حيث البروتينات المرتبطة بها هي tau، وα-synuclein، وTDP-43، وFUS/FET.
يؤدي تجميع هذه البروتينات غير الطبيعية إلى تكوين تشابكات ولويحات تسبب التنكس العصبي. أحد البروتينات الأكثر شيوعًا المرتبطة بالأمراض التنكسية العصبية هو أميلويد بيتا، والذي غالبًا ما يتم اكتشافه على أنه بروتين متراكم مع تاو في مرض الزهايمر.
تم تحديد بروتينات الأميلويد والتاو كأهداف علاجية من خلال البحث. يعد العلاج المناعي هو النهج الأكثر تقدمًا في مرحلة تطوير الأدوية لمعظم هذه الأهداف، لكن اللقاحات والأجسام المضادة المتوافقة مع البشر تستهدف أيضًا البروتينات المرتبطة بالمرض.
دخلت أدوية الزهايمر التجريبية التي تستهدف بروتين تاو في التجارب السريرية هذا العام. وستتم دراستها على مدى السنوات العشر القادمة كجزء من دراسات وحدة تجارب شبكة الزهايمر الموروثة (DIAN-TU). كما حقق الجسم المضاد الواعد، gantenerumab، الذي يستهدف الأميلويد، نجاحًا في المرحلة 2/3 من التجربة السريرية في إطار نفس البرنامج.
ترتبط لويحات الأميلويد بعدة الأمراض التنكسية العصبية وهذا يعني أن العلاجات الناجحة توفر الأمل في إمكانية علاج حالات مماثلة.
المزود الرائد عالميًا للتكنولوجيا المؤتلفةيلعب
مصدر الفيديو: شركة Sino Biological Inc.
العديد من الأدوية التي تستهدف الأميلويد β (Aβ) في مرض الزهايمر (AD) لم تثبت فعاليتها السريرية. فهل يشير ذلك إلى ضرورة اكتشاف أهداف جديدة؟ ما هو الوضع الحالي في هذا الصدد؟
تم وصف لويحات الأميلويد لأول مرة في المرضى الذين يعانون من الخرف في القرن التاسع عشر. منذ ذلك الحين، تمت دراسة بروتين أميلويد- بيتا (Aβ)، الذي يعزز تكوين هذه اللويحات، وتمت ملاحظته كخطوة حاسمة في التسبب في العديد من الأمراض التنكسية العصبية، وخاصة مرض الزهايمر.
ومع ذلك، فإن معظم العلاجات التي تستهدف Aβ لم تكن ناجحة سريريًا. وقد أثار هذا فكرة أن أحداث التجميع هذه قد تكون مسبوقة، والأهم من ذلك، أنها تهيمن عليها أحداث مهمة أخرى تنظم هذا البروتين.
تحدت دراسة حديثة نُشرت في Nature Neuroscience التسلسل المقبول تقليديًا للأحداث التي تؤدي إلى تكوين اللويحة، حيث يُعتقد أن Aβ يؤدي إلى تأثير الدومينو للتنكس العصبي.
وبدلاً من ذلك، ربطت هذه الدراسة بين خلل الالتهام الذاتي وتكوين لوحة الأميلويد مع أدلة قوية في الجسم الحي من خمسة نماذج مختلفة من الفئران. وهذا يتطلب المزيد من التحقيق لتحديد الهدف الرئيسي الذي يمكن التحقق من صحته وتوسيع نطاقه إلى التجارب السريرية.
التجميع المشترك مع Aβ يجعل تاو أيضًا هدفًا علاجيًا مفضلاً. الدراسات السريرية لبروتين تاو كهدف للأجسام المضادة أو الكواشف المشعة في التصوير المقطعي بالإصدار البوزيتروني (PET) تجعله مرشحًا بديلاً قويًا. من بين جميع التجارب السريرية التي ركزت على مرض الزهايمر، ركز 40% منها على Aβ و18% على تاو.
يتم اختبار بعض مثبطات الجزيئات الصغيرة بحثًا عن أهداف في الحماية العصبية، والالتهاب العصبي، وعوامل النمو، ومسارات التمثيل الغذائي العصبي والقلب والأوعية الدموية، بما في ذلك جزيئات مثل عوامل IL-6، وIFNGR1، وp75NTR، وAPOE، وGSK3β، وADRA2B، وCSF.
ما هي النماذج والأدوات واستراتيجيات البحث المستخدمة لاكتشاف أهداف الدواء في الأمراض التنكسية العصبية؟
تقارن الأساليب التقليدية لاكتشاف الأدوية الأفراد المصابين بمجموعات المراقبة لتحديد الاختلافات في الأعراض والفسيولوجية والوراثية لتحديد الحالات المرضية.
تركز الأساليب الجديدة على التقييم الجيني والتشريحي للمجموعات العصبية الضعيفة والمقاومة من نفس الفرد للعثور على التفرد الفسيولوجي والجيني الذي يجعل منطقة واحدة عرضة للإصابة بالأمراض والأخرى محمية من التسبب في المرض.
الدراسات الحالية أكثر شمولاً. فبدلاً من مجرد فحص مرحلة واحدة من المرض، يجب عليهم تلخيص المراحل قبل وبعد ظهور المرض بالإضافة إلى مسار المرض.
يتم استخدام أساليب إنتاجية أعلى، بما في ذلك تحليل التعبير الجيني الكامل وتوصيف الحمض النووي الريبي (RNA) على نطاق الجينوم.
تُستخدم نماذج السيليكو والاستراتيجيات التجريبية لاكتشاف أهداف الدواء لتوفير الوقت وتكلفة التجارب على مجموعات البيانات الكبيرة الناتجة عن تسلسل الجيل التالي وتصوير الأعصاب على نطاق واسع.
يتم دمجها مع الالتحام الجزيئي للتنبؤ بالتشكل الجزيئي وتحسين التفاعلات الدوائية المستهدفة لمكتبات كبيرة من المركبات قبل نقل مجموعات مختلفة من الأدوية الجزيئية واختبارها في الجسم الحي.
تهدف هذه الاستراتيجيات إلى سد الفجوة الكبيرة بين تصميم وإنتاج واختبار الأدوية الفعالة للأمراض التنكسية العصبية.
ما هو التقدم المحرز في المؤشرات الحيوية ومراقبة الأمراض التنكسية العصبية؟
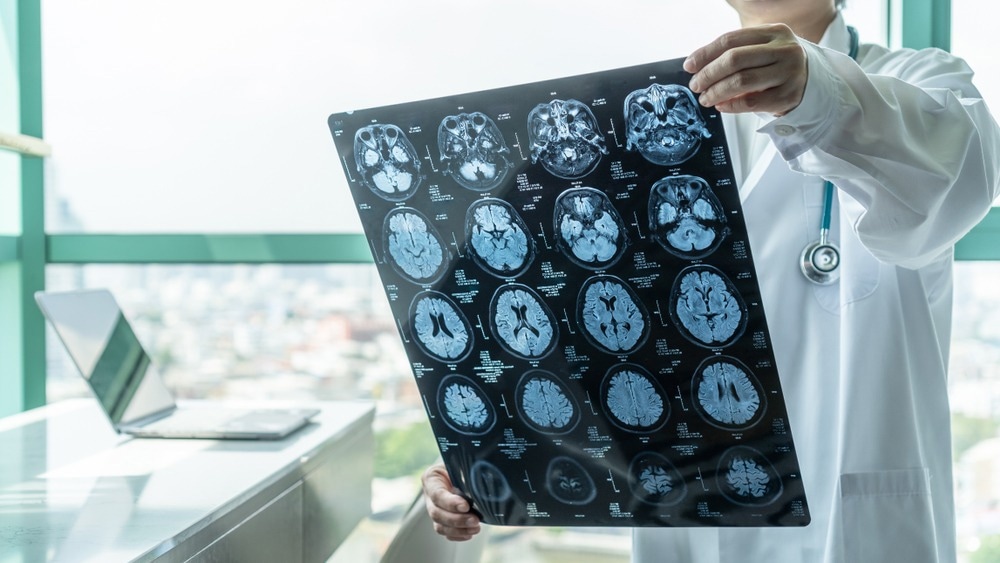
يعد التشخيص المبكر أمرًا بالغ الأهمية لتوفير خطط علاجية جيدة التصميم ومناسبة لمنع تطور المرض. المؤشرات الحيوية الحالية في الأمراض التنكسية العصبية هي بشكل رئيسي لويحات أميلويد بيتا وتشابكات تاو، والتي يتم اكتشافها في التصوير بالرنين المغناطيسي (MRI) والتصوير المقطعي بالإصدار البوزيتروني (PET).
مصدر الصورة: تشينابونج/Shutterstock.com
لقد حسنت هذه العلامات بشكل فعال تشخيص ونتائج علاج مرض الزهايمر. ومع ذلك، فإن المؤشرات الحيوية الواعدة مثل TREM2 وα-synuclein وSV2A لم تظهر خصوصية وحساسية كافية في الاختبارات السريرية ولا تزال قيد التحقيق.
يُقترح أيضًا استخدام مستويات اليوبيكويتين كمؤشرات حيوية لمراقبة تطور المرض، جنبًا إلى جنب مع ضوء الخيط العصبي، وFYN، وBACE1.
خلال الوباء، تم إحراز بعض التقدم الكبير في إنشاء المؤشرات الحيوية القائمة على الدم. يمكن لاختبارات الدم هذه الكشف عن مرض معيّن مفسفر شكل تاو في الدم.
يمكن اكتشاف هذه المؤشرات الحيوية في وقت مبكر من المرض، مما يعني أن لديها القدرة على أن تكون تشخيصًا جيدًا وتمنع تطور المرض.
ما الذي يخبئه المستقبل لاكتشاف وتنفيذ المؤشرات الحيوية الجديدة في الأمراض التنكسية العصبية؟
في الآونة الأخيرة، تتزايد باطراد دراسة جزيئات الالتهابات العصبية والأوعية الدموية العصبية كمؤشرات حيوية محتملة. بعض المؤشرات الحيوية وأهداف الأدوية المقترحة هي TREM2 وGFAP وMCP-1 وMAPK1 وVEGFR1 وFGFR1.
يهدف استهداف هذه الجزيئات إلى تقليل الالتهاب العصبي، وتحسين وظائف الحاجز الدموي الدماغي، ومنع التنكس العصبي.
مع زيادة فهمنا للتسبب في أمراض التنكس العصبي، تتحول استراتيجية العلاج نحو تعزيز آليات الحماية العصبية للخلايا. تساعد عوامل النمو مثل BDNF وNGF وGDNF الخلايا العصبية على البقاء والمحافظة عليها وتجديدها، مما يجعلها علاجات محتملة للأمراض التنكسية العصبية.
تجري حاليًا تجارب سريرية على GDNF (علاج لمرض باركنسون)، وNGF (علاج لمرض الزهايمر)، وBDNF (علاج لمرض الزهايمر ومرض باركنسون). عندما يتعلق الأمر بتصوير الأعصاب وعلاج أمراض التنكس العصبي، فإن روابط PET الجديدة غير الغازية الخاصة بحالة الخلية تتمتع بإمكانات هائلة.
تساعد Sino Biological العلماء على تطوير الأبحاث في مجال أمراض التنكس العصبي من خلال توفير بروتينات مؤتلفة عالية الجودة، وأجسام مضادة، ومجموعات ELISA، ومنتجات جينية، وخدمات CRO.
عن الدكتور ماسي![]()
حصلت الدكتورة ماسي على درجة البكالوريوس من جامعة هيوستن-وسط المدينة وعلى درجة الدكتوراه. في العلوم الجزيئية والطبية الحيوية التكاملية من كلية بايلور للطب. ركزت أطروحتها على إنشاء برنامج تنظيمي بعد النسخ يتم التحكم فيه بالعقاقير في نقائل سرطان الثدي. وهي تعمل حاليًا كمدير مساعد للمنتجات في شركة Sino Biological US Inc. في هيوستن. وهي مهتمة بالتقدم العلمي في اكتشاف الأدوية والعلاج المناعي للسرطان.
أمشركة سينو البيولوجية
العضوية الصينية هي المورد الدولي ومزود الخدمة للكواشف. تتخصص الشركة في إنتاج البروتينات المؤتلفة وتطوير الأجسام المضادة. يتم تطوير وإنتاج جميع منتجات Sino Biological بشكل مستقل، بما في ذلك البروتينات المؤتلفة والأجسام المضادة واستنساخ cDNA. Sino Biological هو متجر الخدمات التقنية الشامل للباحثين لمنصات التكنولوجيا المتقدمة التي يحتاجون إليها لتحقيق التقدم. بالإضافة إلى ذلك، توفر شركة Sino Biological لشركات الأدوية وشركات التكنولوجيا الحيوية خدمات تكنولوجيا الإنتاج قبل السريرية لمئات من مرشحي أدوية الأجسام المضادة وحيدة النسيلة.
الأعمال الأساسية لشركة Sino Biological
تلتزم شركة Sino Biological بتوفير بروتينات مؤتلفة وكواشف الأجسام المضادة عالية الجودة، وبكونها متجرًا شاملاً للخدمات التقنية للباحثين في علوم الحياة حول العالم. يتم تطوير جميع منتجاتنا وإنتاجها داخليًا. كما نقوم بتزويد شركات الأدوية والتكنولوجيا الحيوية بخدمات تكنولوجيا الإنتاج قبل السريرية لمئات من الأدوية المرشحة للأجسام المضادة وحيدة النسيلة. تتوافق مؤشرات مراقبة جودة منتجاتنا مع المتطلبات الصارمة للعينات المخصصة للاستخدام السريري. يستغرق الأمر بضعة أسابيع فقط حتى نتمكن من إنتاج من 1 إلى 30 جرامًا من الأجسام المضادة وحيدة النسيلة المنقاة من التسلسل الجيني.
سياسة المحتوى المدعوم:ينشر موقع News-Medical.net المقالات والمحتوى ذي الصلة، والذي قد يأتي من مصادر لدينا معها علاقات تجارية حالية، بشرط أن يضيف هذا المحتوى قيمة إلى روح التحرير الأساسية لـ News-Medical.Net، والتي تتمثل في تثقيف وإعلام زوار الموقع المهتمين بالأبحاث الطبية والعلوم والأجهزة الطبية والعلاجات.
.

 Suche
Suche
 Mein Konto
Mein Konto